Vaccin Ixchiq contre le chikungunya : un nouveau bilan de l'ANSM fait le point sur les effets indésirables
L'Agence nationale de sécurité du médicament et des produits de santé (ANSM) a publié ce lundi un nouveau bilan concernant le vaccin Ixchiq contre le chikungunya. Depuis le début de la vaccination, 62 cas d'effets indésirables ont été déclarés sur le territoire français, dont 21 cas qualifiés de graves. Sur la période du 2 juin au 31 août 2025, l'agence a enregistré 15 nouveaux cas d'effets indésirables, incluant trois cas graves.
Des déclarations tardives expliquent les nouveaux signalements
Selon l'ANSM, ces nouveaux cas résultent principalement de déclarations tardives concernant des vaccinations effectuées avant fin avril 2025. Cette période correspond à la suspension des injections pour les personnes âgées, une mesure prise en raison de signalements d'effets secondaires graves chez cette population vulnérable. L'agence précise qu'aucun nouveau décès n'a été enregistré dans ce dernier bilan.
Un parcours semé d'embûches pour le vaccin Ixchiq
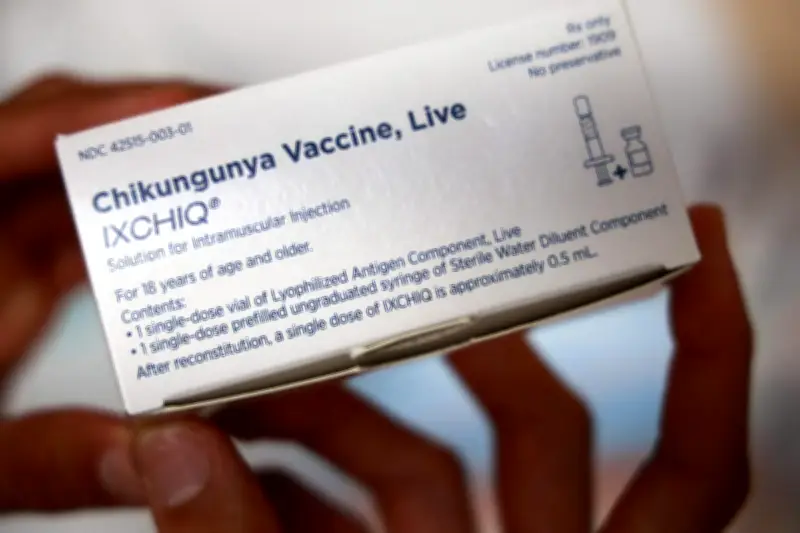
Le vaccin Ixchiq, développé par le laboratoire Valneva, est l'un des rares produits disponibles contre le chikungunya. Cette maladie virale, transmise par le moustique tigre, provoque des fièvres et des douleurs articulaires potentiellement invalidantes. L'année 2025 a été particulièrement mouvementée pour ce vaccin, avec plusieurs suspensions et réévaluations.
En France, le déploiement du vaccin a été perturbé outre-mer suite à plusieurs signalements d'effets graves, tous survenus chez des personnes âgées. Au moins un décès a été rapporté dans le département de la Réunion, frappé début 2025 par une épidémie majeure de chikungunya. Face à ces événements, la France a suspendu l'utilisation du vaccin pour les plus de 65 ans, une mesure rapidement suivie par l'Union européenne.
Une réautorisation européenne mais des contre-indications maintenues en France
L'Union européenne a toutefois réautorisé le vaccin Ixchiq dès juillet 2025, estimant que les effets secondaires observés ne remettaient pas en cause son intérêt contre une maladie particulièrement à risque pour les personnes âgées. Malgré cette décision européenne, la France a annoncé que le vaccin restait contre-indiqué aux seniors en attendant une nouvelle évaluation prévue début 2026.
L'ANSM rappelle également que le vaccin est contre-indiqué chez les personnes dont le système immunitaire est affaibli par une maladie ou un traitement médical. Cette mise en garde fait suite à un nouveau cas de mésusage signalé chez un patient immunodéprimé.
Des risques spécifiques identifiés et surveillés
L'évaluation européenne a confirmé l'existence d'un risque rare d'encéphalopathie et d'encéphalite pour les personnes âgées présentant des maladies associées, avec trois cas signalés à ce jour. Cette information est désormais stipulée sur la notice du médicament.
Par ailleurs, le risque potentiel de méningite aseptique post-vaccination, déjà identifié pour les seniors, fait désormais l'objet d'une surveillance étendue. Un cas rapporté chez un jeune adulte en bonne santé a conduit l'ANSM à renforcer la vigilance sur cette population.
Aux États-Unis, la licence du vaccin Ixchiq a été suspendue fin août 2025 après quatre nouveaux cas d'effets indésirables graves. Cette décision s'inscrit dans un contexte d'inflexion vaccino-sceptique de la politique sanitaire de l'administration Trump.









